Caractéristiques à l'inclusion et devenir des patients
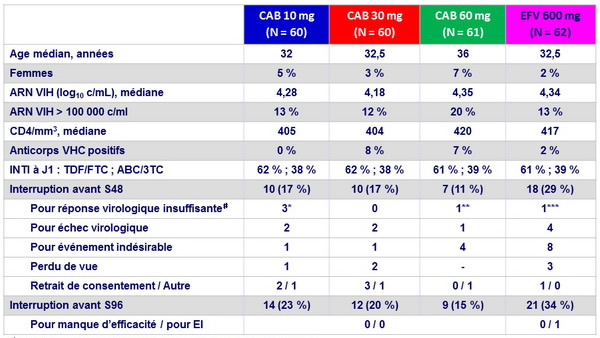
# ARN VIH à S20 : * : 51, 107, 189 c/ mL ; ** : 108 c/ mL ; *** : 146 c/ mL
ARN VIH < 50 c/ml (ITT-E, snapshot)
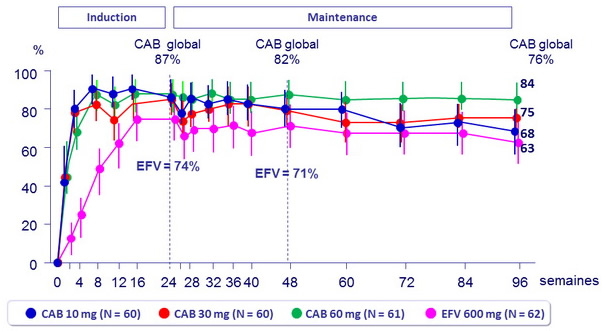
Résultats à S96, ITT -ME , snaphsot
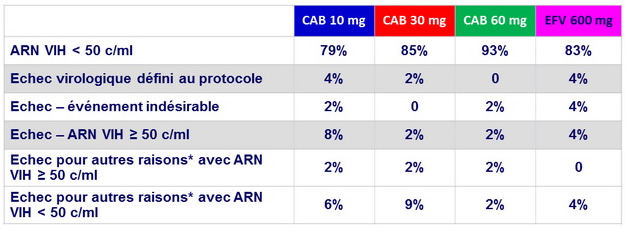
* Autres raisons: données manquantes , déviation au protocole , non observance, perdu de vue , retrait du consentement , décision investigateur , modification du traitement ARV, inéligible pour la phase de maintenance
Echec virologique défini au protocole (EVDP)
- Non réponse : diminution < 1 log 10 c /ml de ARN VIH à S4, sauf si < 400 c/mL ; ou ARN VIH ≥ 200 c /ml à partir de S16
- Rebond : ARN VIH ≥ 200 c /ml après avoir été confirmé < 200 c /ml; ou > 0 , 5 log 10 c /ml au dessus du nadir (la valeur la plus précoce ≥ 200 c /ml)
- Dans tous les cas , nécessité dconfirmation sur un second prélévement
Echecs virologiques (EVDP)
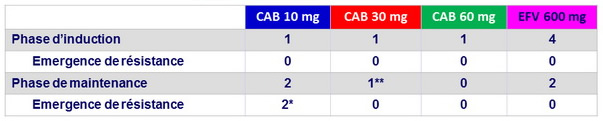
* CAB 10 mg : é mergence de mutation INNTI ( E138Q) et INI (Q148R) à S48 ; CAB FC = 3, RPV FC = 2 ; CAB 10 mg : émergence de mutations de résistance INNTI ( K101K/E + E138E/A) mais pas INI
Un patient supplémentaire sous CAB 10 mg : échec à S48 non confirmé, mutation à INNTI (K101K/E + E138E/K), pas de mutation à INI
** CAB 30 mg : EVDP à S36 sans émergence de mutation INNTI ( intégrase non amplifiée)
Evénements indésirables
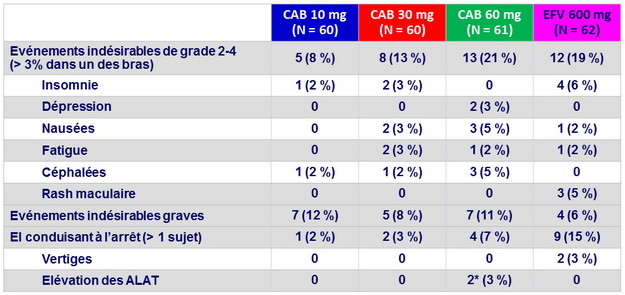
*
2 sujets avec stéato-hépatite ont présenté des élévations asymptomatiques de grade 4 des ALAT (critère d'arrêt pour toxicité hépatique) avec des taux normaux de bilirubine, à S4 et S8, résolutives à l'arrêt des produits de l'essai.
Anomalies biologiques
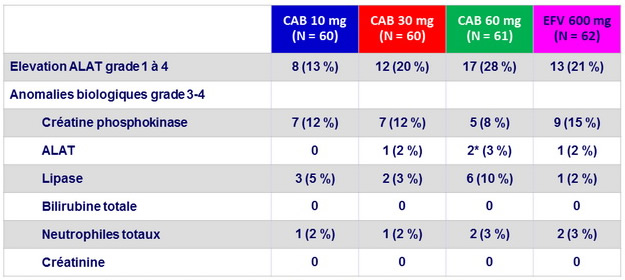
*
2 sujets avec stéato-hépatite ont présenté des élévations asymptomatiques de grade 4 des ALAT (critère d'arrêt pour toxicité hépatique) avec des taux normaux de bilirubine, à S4 et S8, résolutives à l'arrêt des produits de l'essai.



