Estudios comparativos para TARV de primera línea desde 2006
Comparación de INNTR vs IP/r
ACTG A5142: [(EFV vs LPV/r) + 2 INTR] vs EFV + LPV/r
Artículo original : N Engl J Med. 2008 May 15;358(20):2095-106 - SA Riddler
Última actualización :
16/01/2009
Pr Pedro Cahn
University of Buenos Aires
Buenos Aires, Argentina
- Estudio randomizado a 96-semanas comparando 3 regímenes para terapia inicial de HIV
- Menos fallo virológico con EFV + 2 INTR que con LPV/r + 2 INTR
- Régimen ahorrador de INTR de EFV + LPV/r: eficacia virológica similar a EFV + 2 INTR pero más frecuencia de resistencia INNTR y alteraciones lipídicas
- Tendencia no significativa hacia un menor tiempo hasta fallo del régimen con LPV/r + 2 INTR comparado con EFV + 2 INTR
- Sin diferencia significativa entre los 3 grupos en el tiempo hasta toxicidad limitante por tratamiento
- Menores incrementos de recuento de CD4 con EFV + 2 INTR comparado con los 2 grupos de LPV/r
- Emergencia de resistencia a INTR sin diferencia significativa entre EFV + 2 INTR y LPV/r �+ 2 INTR; mutaciones a 2 clases droga significativamente más frecuentes con EFV + 2 INTR; fallo de EFV + INTR asociado con alta frecuencia de resistencia a INNTR; fallo de LPV/r �+ 2 INTR no asociado con resistencia a LPV
- Este estudio muestra moderada superioridad en eficacia de EFV + 2 INTR comparado con �LPV/r + 2 INTR para terapia inicial de la infección por HIV-1
- Los resultados resaltan la complejidad para elegir la terapia inicial con la necesidad de tomar en consideración muchos factores, incluyendo respuesta virológica e inmunológica, tolerabilidad, toxicidad a corto y largo plazo, y las consecuencias de resistencia asociadas con el fallo virológico
Diseño :
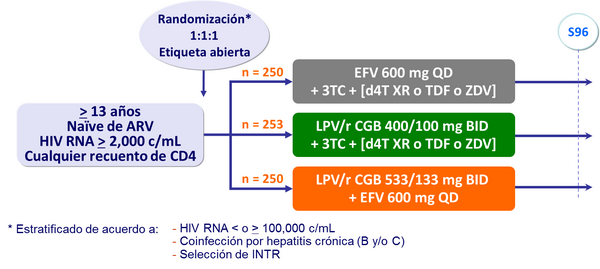
- 3TC = 300 mg QD o 150 mg BID, en todos los pacientes
- 2°INTR (d4T XR 100 mg BID [75 mg si < 60 kg] o TDF [300 mg QD] o ZDV 300 mg BID) seleccionado por el investigador antes de la randomización
- Seguimiento = 96 semanas después de enrolar al último paciente
Objetivos :
- Tiempo hasta el fallo virológico: falta de supresión de HIV RNA en 1 log10 c/mL o rebote antes de S32, o falta de supresión de HIV RNA a < 200 c/mL, o rebote después de S32. Se requirió confirmación de fallo virológico dentro de las 4 semanas. Si faltaba la muestra de confirmación, se incluyó el caso como fallo
- Tiempo hasta el fallo del régimen: el primero de ya sea fallo virológico o suspensión relacionada a toxicidad de cualquier componente de el régimen de tratamiento randomizado inicialmente
Análisis :
- Análisis por ITT estratificado de acuerdo a los 3 factores de randomización, incluyendo todos los pacientes que recibieron al menos una dosis de la droga en estudio
- Si suspensión por intolerancia, el seguimiento continuó para la ocurrencia de fallo virológico
- Si no hubo fallo virológico o del régimen, los datos fueron censados en la última visita del estudio
- Datos faltantes debido a evaluaciones faltantes, pérdida de seguimiento, o censo fueron ignorados
- Poder de 85% para detectar una reducción de 56% en el riesgo de fallo virológico
- Poder de 90% para detectar una reducción de 52% en el riesgo de fallo de régimen
- Puntos finales primarios evaluados con Kaplan-Meier (significancia estadística de razones de riesgo entre grupos de estudio: p < 0.014)
Características basales :
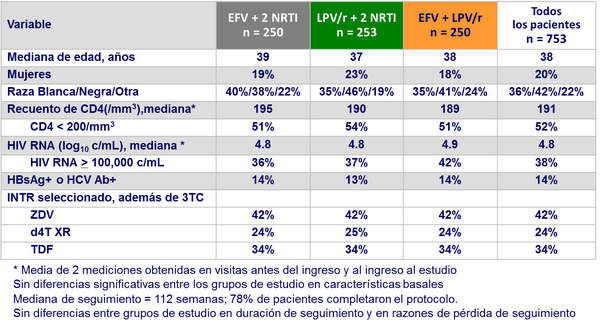
* Media de 2 mediciones obtenidas en visitas antes del ingreso y al ingreso al estudio Sin diferencias significativas entre los grupos de estudio en características basales
Mediana de seguimiento = 112 semanas; 78% de pacientes completaron el protocolo. Sin diferencias entre grupos de estudio en duración de seguimiento y en razones de pérdida de seguimiento
Probabilidad de no fallo virológico (%) :
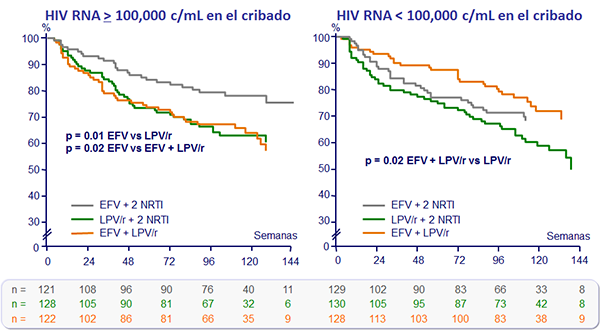
HIV RNA < 50 c/mL :
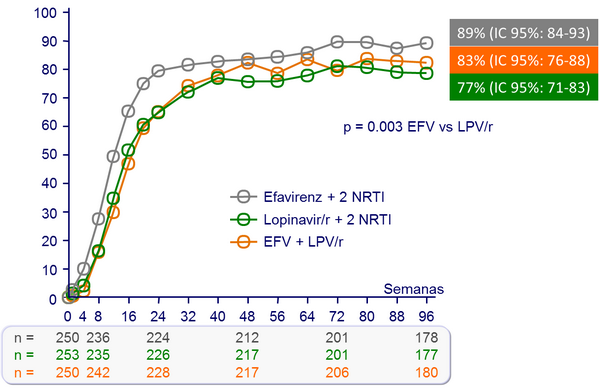
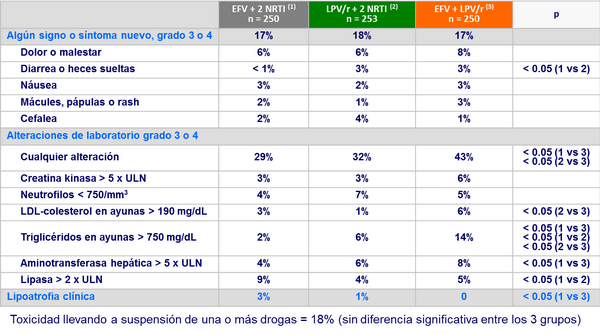
Eventos clínicos o alteraciones de laboratorio grado 3 o 4 :
 Regresar al índice de materias Regresar al índice de materias
|



