Essais cliniques comparatifs pour le traitement antirétroviral de 1ère ligne depuis 2006
Comparaison des IP vs IP
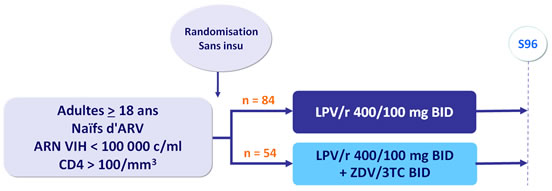
Etude MONARK : monothérapie de LPV/r BID �vs LPV/r BID + ZDV/3TC
Article original : AIDS. 2008 Jan 30;22(3):385-93 - JF Delfraissy
Dernière mise à jour :
18/10/2014
Pr François Raffi
Centre Hospitalier Universitaire
Nantes, France
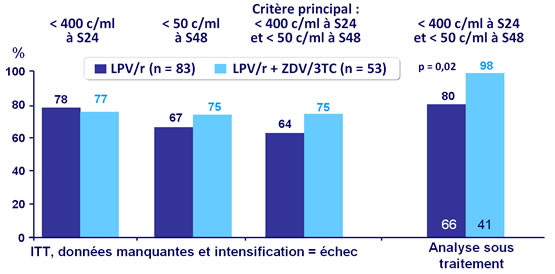
- Chez les patients naïfs d’antirétroviraux, la monothérapie de LPV/r entraîne une suppression virologique inférieure à celle obtenue avec LPV/r + ZDV/3TC
- La monothérapie LPV/r ne doit pas être proposée pour le traitement antirétroviral de 1ère ligne
Schéma d'étude :
LPV/r administré sous forme de capsules molles
Objectif :
- Critère principal : ARN VIH < 400 c/ml à S24 et < 50 c/ml à S48
- Pas de calcul de puissance en raison de l’effectif limité, et le caractère pilote de l’étude
Caractéristiques à l'inclusion et devenir des patients :
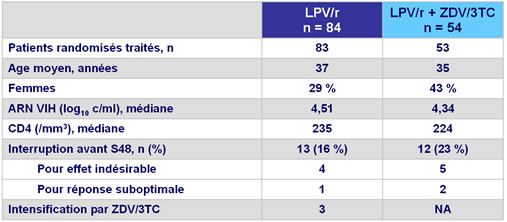
Efficacité (ARN VIH) aux semaines 24 et 48 :
Augmentation médiane des CD4 à S48 : 151/mm3 (LPV/r) vs 159/mm3 (LPV/r + ZDV/3TC) (p = 0,65)
Résistance, tolérance :
- 24/136 patients ont présenté les critères pour une évaluation génotypique de la résistance (rebond de ARN VIH > 500 c/ml) :
- 21/83 avec monothérapie LPV/r et 3/53 avec LPV/r + ZDV/3TC
- Emergence de mutations de résistance aux IP :
- 3/21 patients avec monothérapie LPV/r (L76V, M46I) et aucun avec �LPV/r + ZDV/3TC
- Effet indésirable grave : 12 % avec LPV/r vs 8 % avec LPV/r + ZDV/3TC
- Fréquence similaire dans les 2 groupes des effets indésirables de sévérité au moins modérée, tant cliniques (principalement diarrhée) �que biologiques (élévation des transaminases)
 Retour au sommaire
Retour au sommaire



