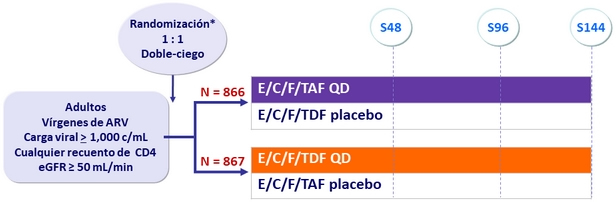
Diseño
*
Randomización estratificada por carga viral ( ≤ o > 100,000 c/ mL ), recuento de CD4 al screening ,
y región geográfica
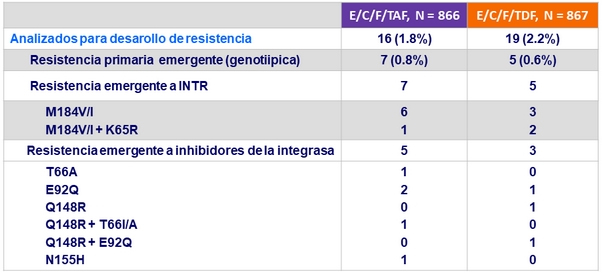
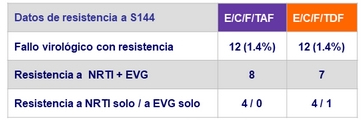
Criterios para las pruebas de Resistencia
- 2 cargas virales consecutivas > 50 c/mL (con la segunda ≥ 400 c/mL) después de alcanzar < 50 c/mL , o carga viral > 400 c/ mL a S48 o ultima visita del estudio
Resistencia a semana 48
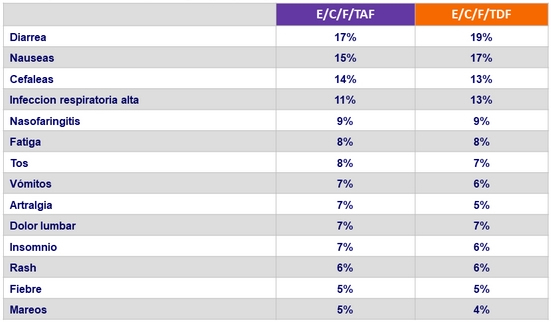
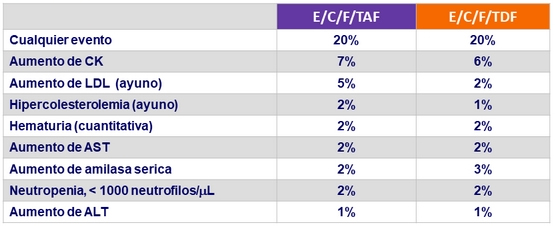
Eventos adversos (todos los grados) ocurriendo en ≥ 5%
de los pacientes en cada grupo (S48)
Eventos adversos determinantes de discontinuación de la droga de estudio
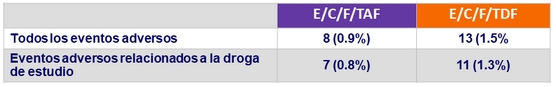
Muerte

Anomalías de laboratorio grado 3 o 4 en ≥ 1% de pacientes en cada grupo (S48)
Discontinuación por evento renal
- E/C/F/TAF = 0
- E/C/F/TDF = 4: fallo renal = 2, disminución del filtrado glomerular GFR = 1, nefropatía = 1
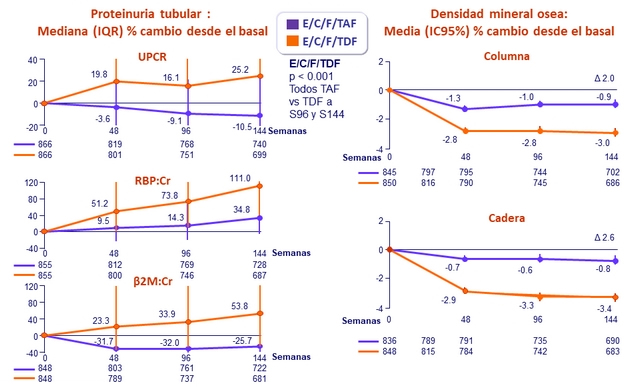
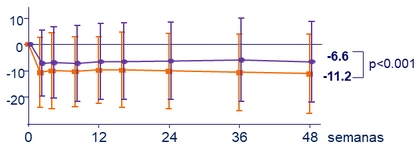
Media (DS) de cambio en eGFR ( Cockcroft-Gault ), mL /min, desde el basal
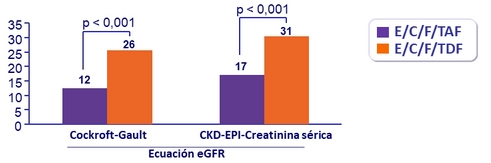
Pacientes con ≥ 25% reducción en el filtrado glomerular
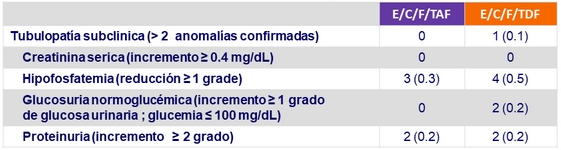
Anomalías renales de laboratorio a semana 48, n (%)
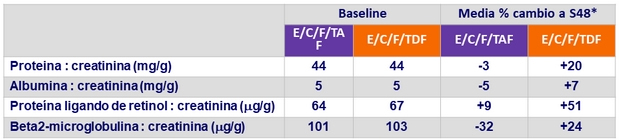
Cambios en la relación cuantitativa proteinuria/creatininuria a semana 48
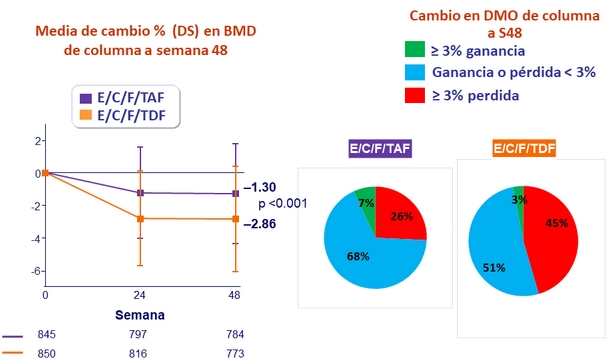
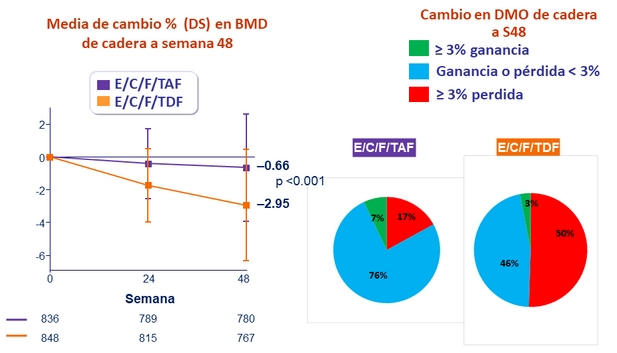
* p < 0.001
para todos
Lípidos en ayunas a semana 48
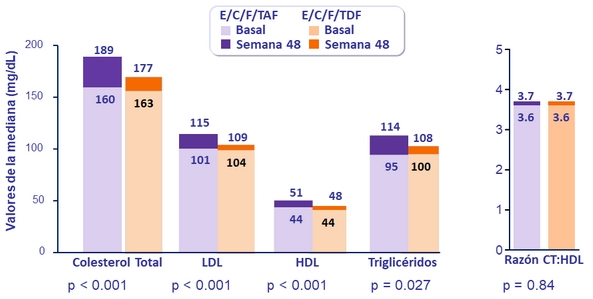
Pacientes iniciando hipolipemiantes : 3.6% E/C/F/TAF vs 2.9% E/C/F/TDF (p = 0.42)
CV < 50 c/mL a S96 y S144
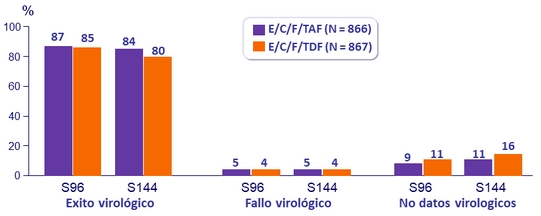
Diferencia en exito virológico (IC95%)
- S96: 1.5% (-1.8 a 4.8)
- S144: 4.2% (0,6 a 7,8) ; p = 0.02
Eventos renales que llevaron a discontinuación del tratamiento a S144
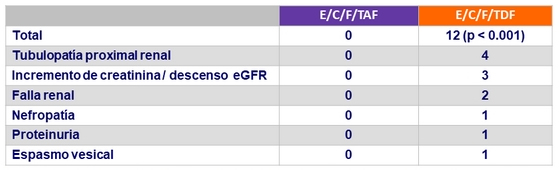
Eventos adversos que llevaron a discontinuación de tratamiento a S144
- 1.3% E/C/F/TAF vs 3.3% E/C/F/TDF (p = 0.01)
Eventos adversos grado 3-4
- No se observaron diferencias entre ambos grupos a S144 excepto por
- Incremento de LDL-colesterol: 11.0% E/C/F/TAF vs 4.8% E/C/F/TDF
- Incremento de c olesterol total: 4.7% vs 2.8%
- Incremento de lipasa : 5.0% vs 8.0%
- Incremento de amilasa : 2.6% vs 5.0%