Mejor tolerabilidad de
- RAL vs ATV/r en pacientes con CV basal < 100 000 c/ml
- RAL vs DRV/r en mujeres
Discontinuación del tratamiento por toxicidad
Incidencia acumulada de fallo virológico o de tolerabilidad
(definición de fallo pre especificada)
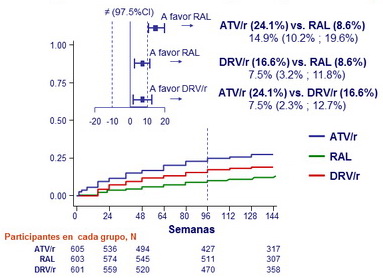
- ATV/r inferior a DRV/r y a RAL
- DRV/r inferior a RAL
CV ≤ 50 copias/ml , independientemente del cambio de TARV (análisis ITT)
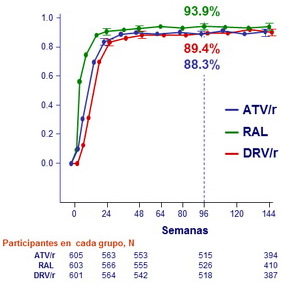
CV ≤ 50 copias/ml recibiendo el TARV randomizado (ITT, análisis snapshot)
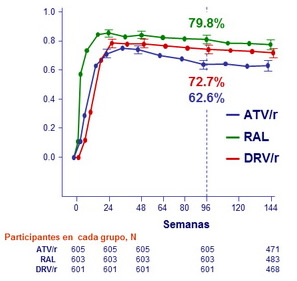
Análisis genotípico de resistencia al fallo virológico
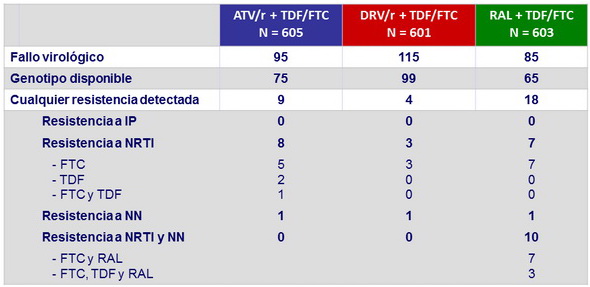
Los pacientes pueden no haber estado en su tratamiento randomizado al momento del fallo
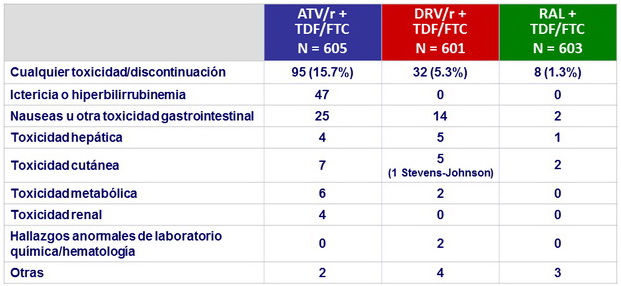
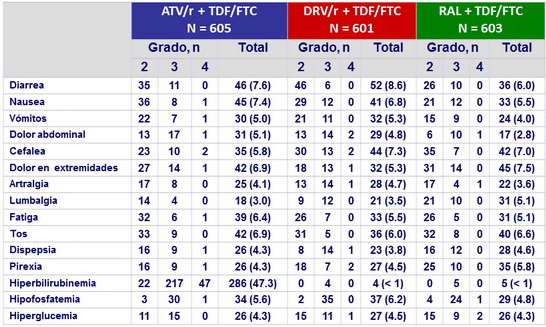
Eventos adversos grado 2 o mas en ≥ 5%
de los pacientes en cada grupo
Otros datos de seguridad
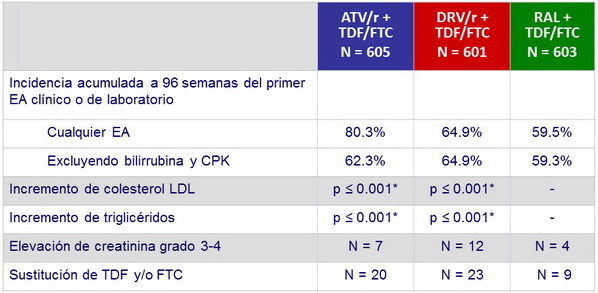
* vs RAL
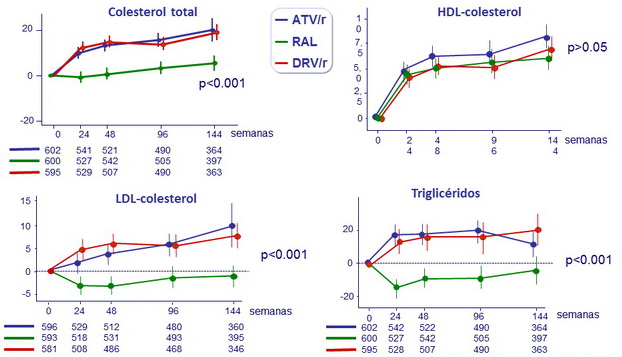
Media (IC 95%) de cambios desde el basal en lípidos en ayunas, mg/dL
Media de cambio porcentual en la masa mineral osea a 96 semanas
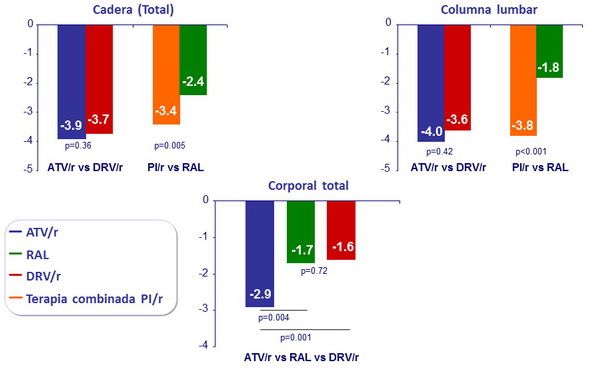
Efecto del CD4 basal y la carga viral en la perdida de masa ósea
- Después de ajustar por edad, sexo, raza/etnia, carga viral basal, índice de masa corporal: no se encontraron asociaciones entre niveles mas bajos de CD4 basal y perdida ósea en la columna lumbar o la cadera total.
- Después de ajuste multivariado , cargas virales mas altas se asociaron con perdida ósea en ambos sitios(columna, −1.53% [95% CI: −2.28 ; 0.77] por cada incremento de 1 log10 c/ml [p < 0.001]; cadera total, −0.82%
[95% CI, −1.51 ; 0.14] por cada incremento de 1 log10 c/ml [p = 0.02])
Análisis multivariado de densidad mineral ósea (DMO) S96
- Factores basales asociados con perdida de DMO en cadera total
- Mayor concentración de hsPCR , IL6, y sCD14
- Factores basales asociados con perdida de DMO en columna lumbar
- Marcadoras de senescencia de CD4+ T- cell y agotamiento de (CD4+CD28−CD57+PD1+)
- Marcadores de activación de CD4+ T- cell (CD4+CD38+HLA-DR+)
Media (97.5%) % del cambio de la composición corporal a S96, ITT : grasa de miembro inferior, tronco
y masa magra (DEXA), grasa visceral (VAT) y subcutánea abdominal (VAT), (TC abdomen)
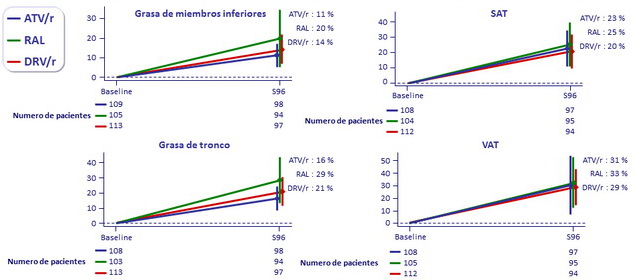
Todos los valores de p (ATV/r vs DRV/r, PI/r vs RAL) no significativos
Mayores incrementos en la circunferencia abdominal se observaron en la rama RAL comparados con la rama DRV/r a S48 y S96 (todas las p ≤ 0.023) pero no comparados con la rama ATV/r
(p ≥ 0.07)
Efecto de la carga viral basal en cambios
en la grasa a S96 en los 3 grupos
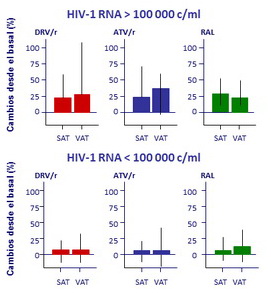
- Cambios en la grasa central correlacionaron con los cambios en la grasa periférica
(r = 0.67 ; p < 0.001)
- Sin cambios en la relación VAT:TAT en cada régimen o entre regímenes
- Mayor incremento en VAT asociado con :
- Menor leptina basal
- Mayor adiponectina basal
- Carga viral
- Mayor incremento en SAT asociado con los mismos factores basales, adicionalmente también con mayores niveles de IL-6
- Mayores incrementos de masa magra asociados con:
- Mayor r HIV RNA, IL-6 y dimero -D,
asi como menor CD4 basal
Cambios en inflamación y activación inmune
- Subestudio A5260S (328 pacientes) : 234 incluidos (HIV RNA < 50 c/ mL
a S24) : 68 en ATV/r, 84 en DRV/r y 82 en RAL
- Biomarcadores plasmáticos de inflamación y coagulación : hsCRP , IL-6, GlycA , D- dimer , sCD14, sCD163, and sIL-2r
- Marcadores celulares sanguíneos : % de subsets de CD38+DR+ of T- cell y %CD14+CD16+ y % de subsets CD14( dim )CD16+
- Cambios en biomarcadores variaron por régimen ARV régimen durante las 96 semanas de seguimiento :
- hsCRP se redujo con ATV/r y RAL
- IL-6 se redujo con RAL
- GLycA se redujo en todos los grupos
- D-dimer se redujo con ATV/r y DRV/r y no cambio con RAL
- Marcadores de activación de células T y sCD163 (pero no CD14 and CD14-+CD16+) declinaron en todos los grupos
- Conclusión : No hay evidencia consistente que la reducción de la inflamación y la activación inmune con el inicio del TARV fuera diferente entre los regímenes basados en RAL o IP



