Phase 2 des nouveaux ARVs
BMS-955176 (maturation inhibitor)
Etude AI468002 : Phase II du BMS-955176
Article original :
Hwang C. CROI 2015, Abs. 114LB
Dernière mise à jour :
01/10/2015
Pr François Raffi
Centre Hospitalier Universitaire
Nantes, France
- Après 24 semaines d'induction avec 2 INTI + CAB, la bithérapie orale de CAB + RPV a permis de maintenir un taux de suppression virologique identique à celui de la trithérapie EFV + 2 INTI sur 96 semaines
- CAB + RPV était bien toléré , avec peu d'évenements indésirables conduisant à l'arrêt du traitement
- La dose de CAB 30 mg QD a été seléctionnée pour les phases III
Schéma de l'étude :
- Phase IIa , randomisée, en double-aveugle, de recherche de dose
- Patients ≥ 18 ans, naïfs d'ARV (≤ 1 semaine de traitement)
ou pré-traités (naïfs d'IP et d'inhibiteur de maturation),
ARN VIH ≥ 5 000 c/ml, CD4 > 200/mm3
- Pour toutes les doses : 8 patients sous BMS-176 qd et 2 sous placebo
- ARN VIH mesuré de J1 à J14, de J17 à J19 et à J24

Caractéristiques des patients
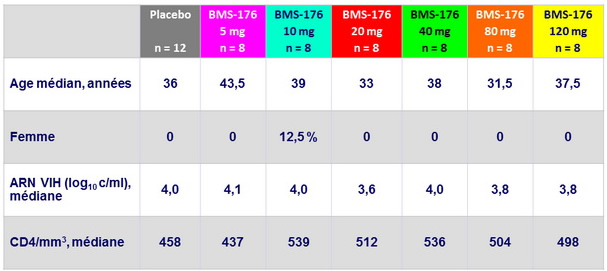
Naïfs d'ARV : 92 %
Réduction médiane maximale de l'ARN VIH depuis J0, log10 c/mL
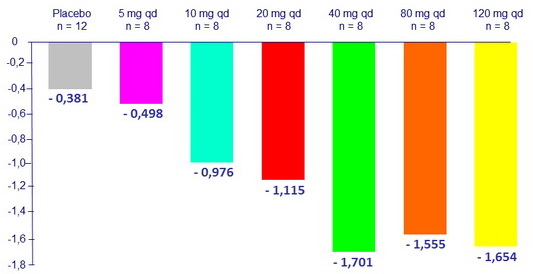
- Réduction médiane moyenne de l'ARN VIH entre J0 et J11 : – 1,4 log10 c/ml
- Relation exposition du BMS-955176 – réponse en faveur d'une activité antivirale dose-dépendante
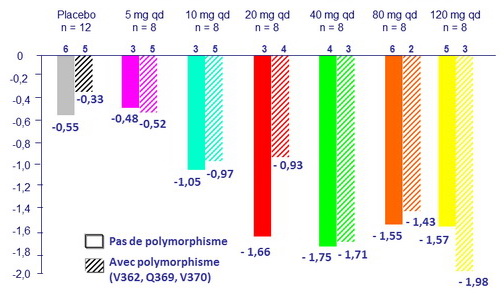
Réduction médiane maximale de l'ARN VIH
en fonction du polymorphisme Gag à J0, log10 c/mL
Evénements indésirables
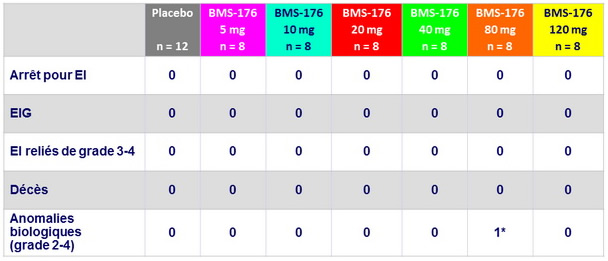
*
Neutropénie transitoire de grade 3, considérée comme liée au traitement
 Retour au sommaire Retour au sommaire
|



